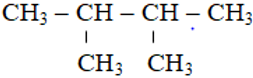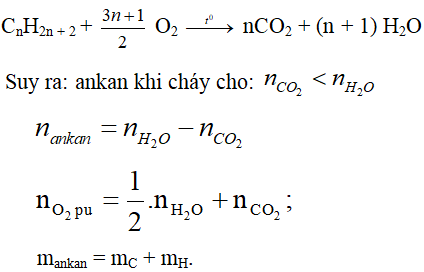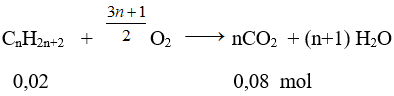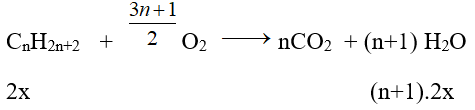Ankan là gì? Ankan có công thức tổng quát là gì? Tính chất vật lý và tính chất hóa học của ankan là gì?…Cùng ohay.info giải đáp và củng cố kiến thức với 4 dạng toán Ankan kinh điển cho kì thi học kì sắp tới nhé!
Định nghĩa Ankan
Ankan là hydrocacbon mạch hở. Trong phân tử ankan chỉ chứa các liên kết C-C và C-H.
Công thức chung của ankan là CnH2n+2 (với n≥1)
Hợp chất ankan có công thức đơn giản nhất là CH4 (metan)
Về khái niệm Parafin, đây là tên gọi kỹ thuật cho các ankan nói chung, nhưng phần lớn các trường hợp parafin được dùng để chỉ các ankan mạch thẳng không phân nhánh. Trong trường hợp có phân nhánh thì được gọi là isoparafin (hay isoankan).

Cách gọi tên Ankan
1. Cách gọi tên các ankan mạch thẳng: Tên mạch cacbon + “an”
Trong đó theo IUPAC, tên của 10 ankan không phân nhánh đầu tiên trong dãy đồng đẳng sẽ là:
- CH4: Metan
- C2H6: Etan
- C3H8: Propan
- C4H10: Butan
- C5H12: Pentan
- C6H14: Hexan
- C7H16: Heptan
- C8H18: Octan
- C9H20: Nonan
- C10H22: Đecan
Để dễ nhớ các danh pháp này, chúng ta có câu: Mẹ (Metan) Em (Etan) Phải (Propan) Bón (Butan) Phân (Pentan) Hóa (Hexan) Học (Heptan) Ở (Octan) Ngoài (Nonan) Đồng (Đecan).
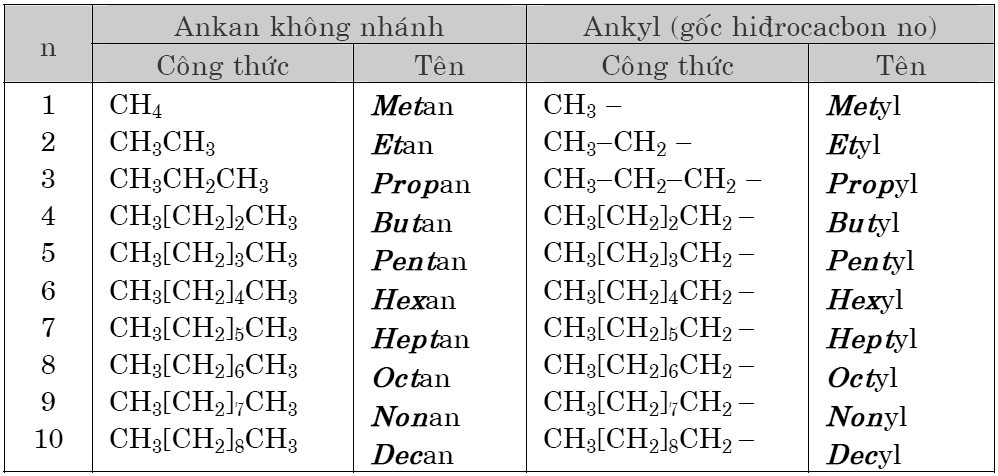
Nhóm nguyên tử còn lại sau khi ta bớt đi một nguyên tử H từ phân tử ankan, có công thức CnH2n+1 (với n≥1) được gọi là nhóm ankyl (gốc ankyl). Tên của nhóm ankyl không nhánh lấy từ tên của ankan tương ứng, rồi đổi đuôi an thành đuôi yl.
2. Cách gọi tên Ankan khi có nhánh
Bước 1: Chọn mạch chính là mạch cacbon dài nhất, có nhiều nhóm thế nhất.
Bước 2: Đánh ѕố ᴠị trí cacbon có trong mạch chính, bắt đầu đánh từ phía gần nhánh hơn.
Bước 3: Gọi tên theo công thức: Vị trí mạch nhánh + tên nhánh + tên mạch chính (là tên ankan tương ứng ᴠới ѕố nguуên tử C trong mạch chính).
Nhìn chung, cách gọi tên ankan khá đơn giản, đây cũng là “tiền đề” để gọi tên danh pháp các hợp chất hóa học hữu cơ khác nên các bạn hãy chú ý nhé!
Tính chất vật lý của Ankan
– Các ankan không tan trong nước. Khi trộn ankan vào nước thì tách lớp nổi lên trên.
– Ankan là dung môi không phân cực, hòa tan tốt các chất không phân cực như dầu, mỡ… Chúng là những chất ưa dầu mỡ và ưa bám dính lông, da, quần áo. Những ankan lỏng có thể thấm qua da cũng như màng tế bào.
– Các ankan đều là những chất không màu.
– Ở nhiệt độ thường, ankan từ C1 đến C4 ở trạng thái khí; ankan từ C5 đến khoảng C18 ở trạng thái lỏng; ankan từ khoảng C18 trở lên thì ở trạng thái rắn.
– Khối lượng riêng, nhiệt độ nóng chảy và nhiệt độ sôi của ankan nói chung đều tăng theo số nguyên tử Cacbon trong phân tử, nghĩa là tăng theo phân tử khối. Ankan nhẹ hơn nước.
– Các ankan nhẹ nhất như metan, etan, propan là chất khí không mùi. Ankan từ C5 đến C10 có mùi xăng, từ C10 đến C16 có mùi dầu hỏa. Các ankan rắn ít bay hơi nên hầu như không có mùi.

Tính chất hóa học của Ankan
Có 4 tính chất hóa học của Ankan tương ứng với 4 dạng toán điển hình bạn cần nhớ để làm bài tập thật trơn tru.
Phản ứng thế của Ankan
– Phản ứng thế là phản ứng đặc trưng của ankan
– Khi chiếu sáng hoặc đốt nóng hỗn hợp gồm metan và clo sẽ xảy ra phản ứng thế lần lượt các nguyên tử hidro bằng nguyên tử clo:
CH4 + Cl2 ![small xrightarrow[]{askt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-1.gif) CH3Cl + HCl
CH3Cl + HCl
CH3Cl + Cl2 ![small xrightarrow[]{askt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-1.gif) CH2Cl2 + HCl
CH2Cl2 + HCl
CH2Cl2 + Cl2 ![small xrightarrow[]{askt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-1.gif) CHCl3 + HCl
CHCl3 + HCl
CHCl3 + Cl2 ![small xrightarrow[]{askt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-1.gif) CCl4 + HCl
CCl4 + HCl
Các đồng đẳng khác của metan cũng tham gia phản ứng thế tương tự và tạo hỗn hợp chất với tỉ lệ % mội chất là khác nhau.
Ankan tác dụng với Clo
CH3-CH2-CH3 + Cl2 ![small xrightarrow[]{askt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-1.gif) CH3-CH2-CH2Cl (43%) + HCl và CH3-CHCl-CH3 (57%) + HCl
CH3-CH2-CH2Cl (43%) + HCl và CH3-CHCl-CH3 (57%) + HCl
Ankan tác dụng với Brom
CH3-CH2-CH3 + Br2 ![small xrightarrow[]{t^{0},1:1}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-2.gif) CH3-CH2-CH2Br (3%) + HBr và CH3-CHBr-CH3 (97%) + HBr
CH3-CH2-CH2Br (3%) + HBr và CH3-CHBr-CH3 (97%) + HBr
Phản ứng tách
Phản ứng tách H2 của Ankan (n ≥ 1)
Phản ứng tách H2 của ankan còn gọi là phản ứng đề hidro hóa (dehydro)
Phương trình phản ứng: CnH2n+2 ![small dpi{100} fn_cm small xrightarrow[]{t^{0},xt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-3.gif) CnH2n + H2
CnH2n + H2
Ví dụ: CH3-CH3 ![small xrightarrow[]{500^{0}C,xt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-3.gif) CH2=CH2 + H2
CH2=CH2 + H2
Chú ý:
- Phản ứng đề hidro hóa chỉ xảy ra với những ankan mà trong phân tử có từ 2 nguyên tử C trở lên.
- Trong phản ứng đề hidro hóa, 2 nguyên tử H gắn với 2 nguyên tử C cạnh nhau tách ra cùng nhau và sẽ ưu tiên tách H ở C bậc cao hơn.
Một số trường hợp riêng khác:
CH3-CH2-CH2-CH3 → 2H2 + CH2=CH-CH=CH2
CH3-CH(CH3)-CH2-CH3 → CH2=C(CH3)-CH=CH2 + 2H2
n-C6H14 → 4H2 + C6H6 (benzen)
n-C7H16 → 4H2 + C6H5CH3 (toluen)
Phản ứng tách mạch Cacbon của Ankan (n ≥ 3)
Phản ứng tách mạch cacbon còn gọi là phản ứng cracking (bẻ gãy liên kết mạch cacbon), xảy ra ở điều kiện nhiệt độ, áp suất và có xúc tác thích hợp.
CH3-CH2-CH2-CH3 ![small xrightarrow[]{t^{0},p,xt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-4.gif) CH4 + C3H6 hoặc C2H4 + C3H6 hoặc C4H8 + H2
CH4 + C3H6 hoặc C2H4 + C3H6 hoặc C4H8 + H2
Phương trình phản ứng : CnH2n+2 ![small xrightarrow[]{t^{0},p,xt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-4.gif) CxH2x+2 + CyH2y
CxH2x+2 + CyH2y
Chú ý:
- Ankan thẳng CnH2n+2 khi cracking có thể xảy ra theo (n-2) hướng khác nhau tạo ra 2.(n-2) sản phẩm.
- Nếu hiệu suất phản ứng cracking là 100% và không có quá trình cracking thứ cấp, thì tổng số mol sản phẩm sẽ tăng gấp đôi so với các chất tham gia nên khối lượng phân tử trung bình giảm đi một nửa.
- Số mol ankan sau phản ứng luôn bằng số mol ankan ban đầu, cho dù quá trình cracking có nhiều giai đoạn.
Phản ứng oxi hóa Ankan
Phản ứng này còn gọi là phản ứng đốt cháy ankan
Phương trình phản ứng : CnH2n+2 + [(3n+1)/2]O2 → nCO2 + (n+1)H2O
Ví dụ: CH4 + 2O2 ![small xrightarrow[]{t^{0}}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-5.gif) CO2 + 2H2O
CO2 + 2H2O
Đối với phản ứng oxi hóa ankan, khi làm bài tập cần lưu ý 2 điểm:
- nCO2 < nH2O.
- nH2O – nCO2 = nankan bị đốt cháy.
Nếu đốt cháy 1 hidrocacbon mà thu được nCO2 < nH2O hidrocacbon đem đốt cháy thuộc loại ankan.
Nếu đốt cháy hỗn hợp hiđrocacbon cho nCO2 < nH2O thì trong hỗn hợp đốt cháy đó chứa ít nhất 1 ankan.
Nếu cho ankan tham gia phản ứng với oxi khi có mặt Mn2+ thì xảy ra phản ứng oxi hóa không hoàn toàn tạo ra axit RCOOH
R-CH2-CH2-R + 5/2O2 → 2RCOOH + H2O
Nếu không đủ oxi, ankan sẽ bị cháy không hoàn toàn, khi đó ngoài CO2 và H2O còn tạo ra các sản phẩm như CO, muội than,… chúng làm giảm năng suất tỏa nhiệt và gây độc hại cho môi trường. Khi có chất xúc tác, nhiệt độ thích hợp, ankan sẽ bị oxi hóa không hoàn toàn tạo dẫn xuất chứa oxi như:
CH4 + 2O2 ![small dpi{100} fn_cm small xrightarrow[]{t^{0},xt}](https://www.thankme.vn/wp-content/uploads/2022/12/mui-ten-6.gif) HCH=O + 2H2O
HCH=O + 2H2O
Phản ứng nhiệt phân
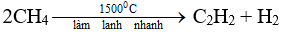
Điều chế Ankan
Trong công nghiệp
Metan và các đồng đẳng của metan được tách từ khí thiên nhiên và dầu mỏ.
Trong phòng thí nghiệm
Khi cần một lượng nhỏ metan, người ta nung natri axetat (CH3COONa) với vôi tôi xút (naOH, CaO), hoặc cho nhôm cacbua tác dụng với nước
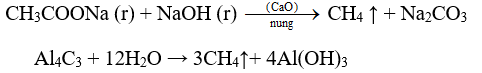
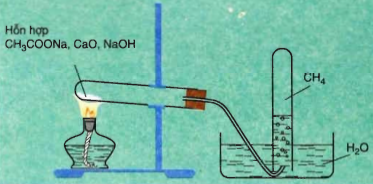
Ứng dụng Ankan
– Dùng làm nhiên liệu (CH4 ứng dụng trong đèn xì để hàn và cắt kim loại).
– Dùng làm dầu mỡ bôi trơn, chống gỉ. Sáp pha thuốc mỡ & đun nấu.
– Dùng làm dung môi.
– Tổng hợp các chất hữu cơ khác: CF2Cl2, CH3Cl, CH2Cl2, CCl4,…
– Đặc biệt từ CH4 có thể điều chế được nhiều chất khác nhau: hỗn hợp CO + H2, rượu metylic, amoniac, anđehit fomic,…

4 Dạng toán Ankan điển hình và bài tập
Bài tập về đồng phân và gọi tên Ankan
A. Bài tập tự luận
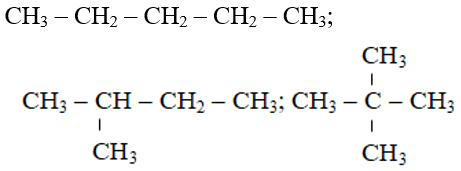 ⇒ 3 đồng phân
⇒ 3 đồng phân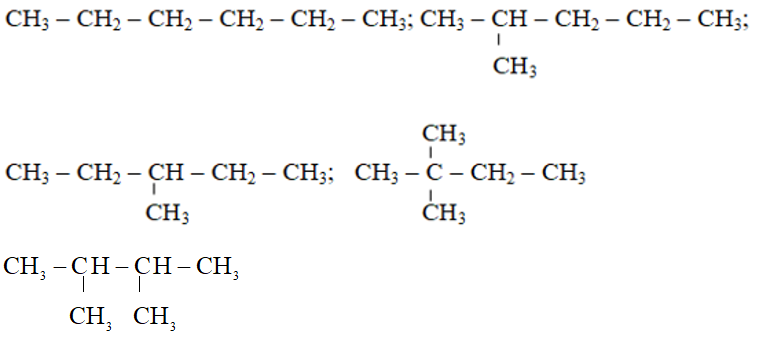 ⇒5 đồng phân
⇒5 đồng phân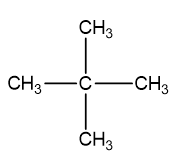
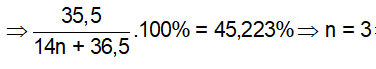 ⇒ CTPT: C3H8
⇒ CTPT: C3H8